

| Remarque : ceci est un travail d'élève au collège. Il n'a pas de caution scientifique, médicale ou autre, et, bien que ces élèves aient fait un travail qui a été accepté dans le contexte scolaire, il ne peut prétendre être une source fiable d'informations ! |
|
|


novembre 1998
I. Introduction
S'il est un sujet d'actualité qui touche à des domaines aussi variés que la science, la politique, le commerce ou l'agriculture, chacun pense évidemment au génie génétique. En effet, les Suisses ont eu l'opportunité au mois de juin dernier de se prononcer démocratiquement et en première mondiale sur cette délicate question du génie génétique. Mais qu'est-ce au fait que le génie génétique ? En une ligne, l'on dirait qu'il définit les procédés mis au point pour modifier le patrimoine génétique d'un organisme vivant (i.e. les végétaux, les animaux et donc l'homme).
Les applications du génie génétique sont essentiellement la santé ou le secteur pharmaceutique (création de médicaments issus de manipulations génétiques, etc..) et le secteur agroalimentaire. Nous allons nous pencher sur ce deuxième cas, car il concerne chacun d'entre nous en tant que consommateurs.
Dans cette optique , nous utiliserons comme exemple l'un des premiers aliments génétiquement modifiés mis sur le marché : la tomate. Une firme américaine a en effet créé une variété de tomate bien particulière nommée " Flavr Savr ".
Nous allons donc étudier les plantes issus des technologies modernes, en analysant les méthodes qui permettent d'obtenir une tomate transgénique. Mais ce travail ne saurait être complet si l'on n'avançait pas de réflexions sur les conséquences de telles manipulations ; quelles sont les risques et les avantages de ces plantes ? qui sont les bénéficiaires de tels projets ? et, somme toute, pourquoi réellement crée-t-on ces nouveaux aliments ?
II. Matériel et méthode
Après avoir fait notre choix du sujet, la recherche d'information a été effectuée. Internet a été notre principal moteur de recherche notamment au moyen du célèbre Altavista mais aussi par les liens hypertextes que M. Lombard nous a mis à disposition. Nous avons donc trouvé un très grand nombre d'article sur le Net à travers plusieurs site très complet sur le génie génétique en général.
Mais il fallut chercher plus loin pour trouver des renseignements plus spécifiques sur notre choix : la tomate Flavr Savr . Nous sommes donc allés dans plusieurs bibliothèques dans l'espoir d'y trouver notre bonheur mais arrivés là-bas, nous n'avons rien découvert de plus sur notre sujet ; les livres récents sont assez rares dans les bibliothèques et comme le génie génétique est un sujet d'actualité, il est plus fructueux de s'intéresser aux journaux et au web.
C'est pourquoi nous avons décidé de mettre les bouchées doubles et de chercher dans notre entourage des personnes spécialisées dans le domaine de la biologie moléculaire, des gens qui en font leur métier et qui pourraient nous faire drôlement avancer
Nous avons donc envoyé un e-mail à Mme Béatrice Pellegrini auteur des articles dans l'Hebdo concernant le Génie Génétique. Mme Pellegrini nous a répondu mais malheureusement elle n'avait pas assez de temps pour l'instant. Mais l'expérience est bonne en comparaison avec des grandes boîtes comme Monsanto, Novartis ou encore Calgene, à qui nous avons également envoyé plusieurs e-mail et qui n'ont pris la peine de nous répondre.
Nous avons aussi visionné une cassette vidéo sur l'agriculture aux Etats-Unis en prenant note de chaque élément intéressant.
Finalement, après le tri des articles en notre possession, avons pu nous mettre au travail et comprendre tout le fonctionnement avant de faire un plan définitif de ce rapport et d'y écrire la première ligne.
III. resultats
Le chapitre suivant présente nos sources d'informations qui nous ont permis d'élaborer le chapitre IV. Parmi les supports d'information, nous avons choisi d'utiliser le plus souvent Internet, car cela permet de rechercher rapidement et de trouver des articles très récents ; de plus, de nombreux quotidiens ont un site sur le Web, ce qui nous a permis de trouver leurs articles sans leur faire de commande. Malgré tout, nous n'avons pas négligé livres, brochures et films.
A. Articles d'Internet
Biotechnologies
Le terme biotechnologies recouvre un ensemble de techniques qui utilisent des micro-organismes, des cellules animales, végétales ou leurs constituants pour produire des substances utiles à l'homme. Les techniques à l'úuvre dans la fermentation relevaient des biotechnologies avant la lettre. En effet, "le terme de fermentation désigne tout processus par lequel des matières organiques - en général de nature végétale sont transformées en produits définis par une action contrôlée de souches de micro-organismes sélectionnés"10. L'utilisation des micro-organismes pour les fermentations est immémoriale. Le fromage, le vin, la bière, le pain ce symbole par excellence de l'aliment - constituent autant d'exemples de l'emploi des fermentations dans le domaine alimentaire. Le processus de panification illustre ainsi une application des biotechnologies traditionnelles : "Prenez 200 épis de blé et vous pouvez extraire 200 grammes de farine. Elle renferme 62 à 64% d'amidon qui, au contact de l'eau, de la levure et après pétrissage, fermente : les enzymes de levure attaquent les chaînes de sucre, ce qui dégage de l'alcool et du gaz carbonique contribuant à gonfler la pâte". De même, le vin est le produit d'un processus de fermentation : "Comment le jus de raisin devint-il un jour du vin ? Sous l'influence de certaines levures, les saccharomyces, poudrant la peau des grains de cette poussière qu'on appelle la pruine ; se multipliant d'une façon extraordinaire en vase clos, les levures provoquent une fermentation alcoolique des grappes écrasées qui emprunte son énergie à l'eau et au sucre du jus. Cette fermentation plus ou moins poussée, de cinq jours à cinq semaines, décolore plus ou moins la peau du raisin, colore le vin en échange et se charge de son tanin, porteur du bouquet"11. Avec le développement spectaculaire de la biologie moléculaire et singulièrement de la génétique, les biotechnologies ont aujourd'hui élargi le champ de leurs possibles applications et les techniques d'amélioration des plantes se trouvent dotées désormais de perspectives nouvelles. Grâce à l'apport du génie génétique, les méthodes de sélection atteignent une précision impensable jusque là, et ce dans des conditions d'efficacité et de sûreté également portées à un niveau supérieur.
Par le biais des biotechnologies, il est désormais possible d'établir la carte génétique d'une espèce végétale afin de trouver la correspondance entre la localisation d'un gène et un caractère agronomique. Ainsi, des chercheurs américains ont démontré la corrélation de certains gènes localisés sur la carte génétique du maïs et des effets positifs sur le rendement. Ce domaine d'application présente un intérêt crucial : il permet en effet de repérer les gènes offrant un caractère d'intérêt. Pour poursuivre l'exemple du maïs, les gènes contrôlant rendement, précocité ou vigueur au départ peuvent de la sorte être repérés dans la carte génétique de la plante. Le suivi de ces gènes permet alors de concevoir beaucoup plus efficacement des variétés nouvelles.
()
La création de plantes génétiquement modifiées
La transgénèse constitue le troisième domaine d'application des biotechnologies. Si les techniques évoquées plus haut permettent d'envisager une amélioration des plantes à grande échelle, la transgénèse autorise l'apport de caractères d'intérêt jusque là inaccessibles à certaines espèces, avec une grande précision.
()
Génie génétique
Le génie génétique "désigne un ensemble de pratiques, de procédés permettant de [...] faire réaliser par un être vivant tout ou partie du programme génétique d'un autre être vivant"12. En d'autres termes, le génie génétique désigne l'ensemble des procédés au moyen desquels il est possible de modifier le patrimoine génétique d'un être vivant.
Principe
Un exemple permet de saisir à la fois le principe et l'intérêt des transferts de gène. Le maïs est exposé aux ravages d'un insecte nuisible : la pyrale. La pyrale est responsable en France de pertes de rendement de l'ordre de 3 à 7% / ha. Or, il existe une bactérie, répondant au nom de Bacillus thuringiensis, présentant une caractéristique digne d'intérêt : celle de produire une protéine (non toxique pour l'homme et les autres animaux) qui détruit les larves de pyrale. Les chercheurs ont pu isoler le gène responsable de ce caractère chez la bactérie. Grâce aux techniques du génie génétique, ce gène a pu être transféré à des plants de maïs, dès lors en mesure de faire la synthèse de la protéine intéressante. Le maïs ainsi transformé offre une résistance nouvelle à la pyrale.
La transgénèse désigne le processus de transfert dans le patrimoine génétique d'un organisme vivant d'un gène qui lui est étranger (le transgène). Ainsi, dans le cas du maïs, le gène bactérien responsable de la synthèse de la protéine détruisant la pyrale, constitue un tel transgène. Son introduction dans le génome du maïs confère à la plante un caractère nouveau de résistance à la pyrale. Ce transgène devient partie intégrante du patrimoine génétique de la plante; il sera alors transmissible à ses descendants, en suivant les lois de la génétique (lois de Mendel).
Il est ainsi possible de transmettre à une plante un caractère intéressant, tel que la résistance à un insecte ou à une maladie, en introduisant dans son patrimoine génétique un transgène exprimant ce caractère. Il importe de saisir ici que le génie génétique ne se substitue pas aux procédés éprouvés d'amélioration des plantes cultivées utilisés en agriculture. Il élargit par contre la gamme des outils disponibles, et ouvre des perspectives jusqu'alors hors de portée. Le gain de temps qu'il procure en fait un outil précieux pour les sélectionneurs, ce qui autorise une réponse rapide aux attentes de l'utilisateur final : le génie génétique permet en effet d'introduire plus rapidement un gène présentant un caractère d'intérêt, avec une précision accrue (on utilise un gène bien défini), dès lors que l'on ne dispose pas du gène porteur du caractère recherché au sein de l'espèce concernée.
Ainsi on ne procède plus par croisements successifs, mais en transférant un gène précis parmi les milliers que compte la plante, ce gène étant à même d'exprimer un caractère désiré. La sélection classique permet d'obtenir une plante améliorée dont les caractères sont identifiés et stabilisés d'une génération à l'autre au terme d'un processus s'étendant sur 8 à 10 ans. L'utilisation du génie génétique peut réduire cette période à 3, voire 4 ans, une fois le gène d'intérêt isolé. La palette des caractères génétiques pouvant être introduits dans une plante s'élargit considérablement puisque le génie génétique permet l'introduction de caractères impossible à réaliser par la sélection classique (le transgène pouvant provenir d'une autre espèce ou d'un micro-organisme).
Le génie génétique et les plantes : les grandes étapes
1973 - Identification du plasmide Ti dans la bactérie Agrobacterium tumefaciens. Ce plasmide permet d'accueillir le gène porteur d'un caractère recherché, qu'il est en mesure d'introduire dans le génome
d'une plante
1983 - Première plante transgénique (tabac) Premier transfert de gène opérationnel réalisé chez un végétal, obtenu simultanément par les équipes de Monsanto et Agrigenetics (USA). L'équipe de Jeff Schell et Marc Van Montagu à Gand obtient des tabacs transgéniques résistant à un antibiotique
1985 - Première plante transgénique résistante à un insecte
1987 - Première plante transgénique tolérante à un herbicide total
1988 - Première plante "pharmacienne". Première céréale transgénique (maïs)
1994 - Premier légume transgénique commercialisé (aux Etats-Unis)
1997 - Premier tabac producteur d'hémoglobine
()
Techniques de transfert de gène
Deux types de techniques complémentaires coexistent : le vecteur biologique et le transfert direct.
a - L'utilisation d'un vecteur biologique
Un plasmide est un "petit ADN circulaire qui se multiplie de manière autonome dans les bactéries. Chaque plasmide peut abriter un fragment d'ADN étranger. Il permet ainsi d'isoler les gènes des êtres vivants"13. Après avoir pénétré dans la plante, une bactérie du sol Agrobacterium tumefaciens transfère une partie de l'ADN du plasmide Ti dans le patrimoine génétique de la plante. C'est sur ce phénomène naturel que repose la transformation par vecteur biologique, le gène porteur du caractère d'intérêt étant substitué au gène bactérien. Le plasmide est alors en mesure de transférer ce gène dans le patrimoine génétique de la plante. Ce type de transformation n'est efficace pour l'instant que chez certaines espèces telles que tabac, colza, tomate, pomme de terre, melon, tournesol. Pour les autres plantes, on utilise un mode de transformation différent : la transformation directe.
b- La transformation directe
Utilisation de la biolistique (projection mécanique d'ADN).
La biolistique consiste à introduire directement de l'ADN dans le noyau des cellules végétales par projection de microbilles métalliques porteuses de cet ADN. Cette méthode qui provoque l'intégration des fragments d'ADN est employée pour le maïs, le blé, le riz, le coton, le soja...
Electroporation ou utilisation d'un agent chimique.
Au moyen d'impulsions électriques (électroporation) ou d'un agent chimique (le polyéthylène glycol), la perméabilité de la membrane cellulaire est augmentée transitoirement. Ceci facilite l'intégration du transgène dans la plante.
()
Les produits issus des biotechnologies
Pour répondre à la diversité des besoins ainsi qu'aux nouvelles exigences des consommateurs, les aliments devront, tout en restant peu coûteux, répondre à ces attentes (meilleur goût, apport de vitamines,...).
Les nouveaux produits
En 1994, une tomate transgénique à maturation retardée a été autorisée à la production et à la vente aux Etats-Unis. Premier d'une série de produits disponibles aujourd'hui outre-Atlantique, cette tomate présentait un avantage en termes de commodité d'emploi. Indépendamment de ce caractère particulier, la variété n'a pas répondu aux attentes des producteurs. Les travaux en cours portent sur l'introduction de ce gène dans des variétés appréciées pour leurs qualités organoleptiques. Cet exemple montre bien que la valorisation d'un transgène dépendra toujours de la qualité génétique du matériel traditionnel concerné. En Europe, la Grande-Bretagne a obtenu l'autorisation d'importer une purée de tomates, à base de tomates transgéniques à longue durée de conservation. Cette purée est vendue sous marque distributeur avec un étiquetage spécifique.
Les produits en cours de développement
a- Une meilleure adaptation à certains usages
Une pomme de terre mieux adaptée à la friture est en cours de développement. Grâce à l'introduction d'un gène de modification de la texture d'amidon chez la pomme de terre, la texture de cette pomme de terre est moins spongieuse. Dès lors, elle absorbe significativement moins d'huile lors de la cuisson.
b- Un meilleur goût
Ainsi que l'explique Mathilde Causse, chercheur à l'INRA : "après avoir travaillé sur la conservation, nous travaillons maintenant sur le goût. Les tomates du futur seront très savoureuses". Un procédé similaire à celui employé pour retarder la maturation de la tomate a permis à une équipe de recherche Ensat-Inra d'obtenir un melon dont la conservation et la teneur en sucre sont augmentées.
c- Des huiles végétales riches en acides gras rares
L'introduction de gènes de désaturases dans les plantes oléagineuses permet d'augmenter la proportion d'acides gras insaturés, particulièrement recherchés en alimentation humaine pour diminuer les risques cardio-vasculaires.
d- Des légumes bénéfiques pour la santé
Une variété de tomates à teneur élevée en b-carotène fait actuellement l'objet de recherche en Europe. Cette vitamine constituerait notamment un élément de prévention du cancer.
Tomate Flavr Savr
Tomate obtenue par l'introduction d'un gène qui inhibe l'effet du gène de maturation. La tomate Flavr Savr se garde plus longtemps; dans le cas idéal, elle peut finir de mûrir au soleil avant d'être mise sur le marché. Aux Etats-Unis et en Grande-Bretagne, elle est vendue sous forme de légume, de purée ou de ketchup. Elle n'est pas (encore) disponible en Suisse.
3. http://www.jouy.inra.fr/actualite/dossiers/ogm.html
Des outils et des méthodes
Le génie génétique permet d'introduire dans une cellule un gène qu'elle ne possède pas. Le fonctionnement de ce gène se traduit habituellement par son expression, c'est-à-dire par la synthèse de la protéine qu'il code. Le génie génétique permet également la suppression ou la modification de l'expression d'un gène déjà présent dans le génome* de la cellule hôte. Le génie génétique peut s'appliquer aux végétaux, aux animaux, aux micro-organismes...
Une plante transgénique est une plante dont le génome a été modifié par l'introduction d'un gène qui peut provenir d'une autre plante, d'une bactérie ou de tout autre organisme. Ce gène peut coder une nouvelle protéine, par exemple un composé toxique pour les insectes ravageurs, une enzyme* qui intervient dans la maturation des fruits, une substance qui bloque la multiplication d'un virus...
Un OGM* (Organisme Génétiquement Modifié) est un organisme vivant dont le génome a été modifié par génie génétique. Toutes les cellules de cet organisme possèdent le gène étranger. C'est pourquoi cette modification génétique est transmissible à sa descendance. Dans le cas d'une plante, l'OGM est la plante transgénique et, par extension, toutes ses parties capables de donner une nouvelle plante (fruits, graines, organes de reproduction végétative).
Les produits dérivés des OGM, n'ayant aucune capacité de reproduction, ne sont pas des OGM, même s'ils peuvent éventuellement contenir le gène introduit ou la protéine codée par ce gène. Par exemple, des plants de colza transgénique résistant à un champignon pathogène sont des OGM, leurs graines aussi. En revanche, l'huile de colza destinée à l'alimentation humaine, ou le tourteau de colza destiné à l'alimentation animale, ne sont pas des OGM, mais des produits dérivés d'un OGM. Compte tenu des procédés de fabrication et de purification, il est probable que la plupart des huiles raffinées que nous consommons ne contiennnent pas de protéines ou d'ADN. Le tourteau, obtenu à partir des résidus de fabrication de l'huile, contient des protéines et de l'ADN. Il peut donc contenir le gène de résistance au champignon pathogène et la protéine codée par ce gène.
Comment obtient-on une plante transgénique ?
1. Repérage d'un caractère intéressant dans un autre organisme vivant (plante, champignon, bactérie...) et identification de la protéine responsable de ce caractère, par exemple un composé toxique pour un insecte ravageur.
2. Identification et isolement du gène codant cette protéine.
3. Réalisation d'une "construction génique" qui contient le gène d'intérêt et des séquences d'ADN (promoteur, terminateur) indispensables à son fonctionnement dans le génome d'une cellule végétale. Ces séquences sont impliquées dans la régulation de l'expression du gène. Elles permettent de cibler le lieu d'expression du gène dans la plante (graines, racines, feuilles...), voire de faire en sorte qu'il ne s'exprime qu'au moment nécessaire, lors de l'attaque d'un insecte ou de l'infection par un virus par exemple. Cette construction contient éventuellement un gène marqueur de repérage des plantes transgéniques (par exemple un gène de résistance à un antibiotique). Cette construction génique est ensuite insérée dans un plasmide bactérien (mini-boucle d'ADN) pour être multipliée.
4. Introduction de la construction génique dans le génome de la cellule végétale par deux méthodes principales :
- transfert biologique : au moyen d'un vecteur, la bactérie du sol Agrobacterium tumefaciens, qui transfère naturellement une partie de son ADN (auquel on a donc ajouté la construction génique à intégrer) dans le génome des plantes.
- transfert mécanique : les constructions géniques, portées par des microbilles de tungstène, sont projetées dans la cellule végétale.
5. Sélection des cellules exprimant le gène ajouté.
6. Régénération de plantes entières à partir de ces cellules. Ces plantes sont testées en serre puis en champ afin de vérifier la conformité de leur développement, la stabilité de l'expression du gène ajouté, sa transmission à la descendance.
Comprendre le fonctionnement des plantes
En permettant d'introduire un gène, ou encore de modifier ou d'inactiver l'expression d'un gène déjà présent, le génie génétique offre la possibilité d'étudier précisément le rôle et la régulation de ce gène dans la vie de la plante (germination, croissance, développement, floraison...). Il permet ainsi de mieux comprendre les mécanismes intimes du fonctionnement végétal avec, en perspective, une meilleure gestion et une meilleure utilisation des plantes. Trois exemples sont ici présentés.
Améliorer les plantes cultivées
Une plante transgénique, dans laquelle a été introduit un gène exprimant un caractère intéressant, par exemple une résistance à une maladie, peut servir à améliorer les plantes cultivées ; elle entre alors dans les schémas habituels de sélection variétale : introduction du gène choisi dans des variétés reconnues pour leur valeur agronomique (précocité, rendement...), par croisements (reproduction sexuée) avec la plante transgénique et sélection des plantes filles qui auront conservé leur qualité agronomique tout en exprimant le transgène*. Le génie génétique ne se substitue pas aux schémas d'amélioration des plantes cultivées utilisés en agriculture. Il constitue un outil supplémentaire pour les sélectionneurs, un outil précieux, car il permet d'introduire plus rapidement un gène intéressant, tout en étant précis puisqu'on utilise un gène bien défini. De plus, il donne accès à un plus grand nombre de gènes et permet de les introduire dans les plantes cultivées même si celles-ci ne se croisent pas avec l'organisme porteur du gène visé (plante d'une autre espèce, micro-organisme...).
Les chercheurs de l'INRA travaillent à l'amélioration des techniques du génie génétique. D'une part, pour apporter encore plus de précision sur le lieu ( feuilles, graines, fruits...) et le moment (lors de l'attaque par un insecte ravageur par exemple) de l'expression du gène dans la plante ; d'autre part, pour mettre en úuvre d'autres gènes d'intérêt, notamment pour lutter contre les maladies virales des plantes. L'utilisation des plantes transgéniques résistantes aux maladies, aux insectes ou aux herbicides pourrait autoriser une réduction des traitements chimiques sur les cultures ou l'emploi de produits moins nocifs pour l'environnement. On peut également envisager l'obtention de plantes transgéniques aux qualités nutritionnelles modifiées.
4. http://isip.com/antisens.htm
Antisense gene
The information necessary to produce proteins in cells is contained in genes. Specific genes contain information to produce specific proteins. The information required for the human body to produce all proteins is contained in the human genome and its collection of more than 100,000 genes. Genes are made up of DNA which contains information about when and how much of which protein to produce, depending upon what function is to be performed. The DNA molecule is a "double helix" -- a duplex of entwined strands. In each duplex, the bases or nucleotides (Adenine, Thymidine, Guanine, Cytosine) are weakly bound or "paired" by hydrogen bonds to complementary nucleotides on the other strand (A to T, G to C). Such highly specific complementary base pairing is the essence of information transfer from DNA to its intermediary, messenger RNA (mRNA), and carries the information, spelled out by the specific sequences of bases, necessary for the cell to produce a specific protein.
During transcription of information from DNA into mRNA, the two complementary strands of the DNA partly uncoil. The "sense" strand separates from the "antisense" strand. The "antisense" strand of DNA is used as a template for transcribing enzymes which assemble mRNA -- a process called "transcription." Then, mRNA migrates into the cell where other cellular structures called ribosomes read the encoded information, its mRNA's base sequence, and in so doing, string together amino acids to form a specific protein. This process is called "translation."
Antisense drugs are complementary strands of small segments of mRNA. To create antisense drugs, nucleotides are linked together in short chains (called oligonucleotides) Each antisense drug is designed to bind to a specific sequence of nucleotides in its mRNA target to inhibit production of the protein encoded by the target mRNA. By acting at this earlier stage in the disease-causing process to prevent the production of a disease-causing protein, antisense drugs have the potential to provide greater therapeutic benefit than traditional drugs which do not act until the disease-causing protein has already been produced.
Antisense drugs have the potential to be much more selective or specific than traditional drugs, and therefore more effective, because they bind to mRNA targets at multiple points of interaction at a single receptor site. Traditional drugs usually bind at only two points of interaction.
The design of antisense compounds also has the advantage of being less complex, more rapid and more efficient than traditional drug design directed at protein targets. Rational drug design usually begins by characterizing the three-dimensional structure of the protein target in order to design a prototype drug to interact with the target. Proteins, however, are complex molecules whose structure is difficult to predict. In contrast, antisense compounds are designed to bind to mRNA whose structures are more easily understood and predicted. Once the receptor sequence on the mRNA is identified, the three-dimensional structure of the receptor site can be defined, and the prototype antisense drugs can be designed.
5. http://trc.ucdavis.edu/Coursepages /PLB105/students /Tomato/reproductive /flavr.html
Genetically Engineered Tomatoes
The phrase "genetic engineering" often provokes negative images in the minds of the American public. Because of movies like Jurassic Park , many people think that altering the genes of organisms will only lead to large, uncontrollable dinosaurs that wreak havoc on a small island off the Costa Rican shoreline. The truth is that genetic engineering is really a tamer science than that portrayed in Jurassic Park . Most genetic engineers are making alterations in just a few genes in certain organisms, rather than creating extinct species from fragments of DNA. While scientists conduct genetic research on a variety of organisms, the ones that genetic engineers are studying for commercial purposes are mostly plants. Scientists are experimenting with many different plants, but the genetic engineering of the tomato has been the the most highly publicized project by far. Calgene, an genetic engineering company in Davis, California, sought to create, through genetic engineering, the perfect tomato.
Supermarket tomatoes are not very tasty compared to garden-grown, vine-ripened tomatoes. Calgene noted this problem and began investigating how they could genetically engineer a tomato that could ripen on the vine and still be transported without being bruised or damaged. After over a decade of research, Calgene perfected the Flavr Savr, their genetically engineered tomato. The scientists have altered the gene on the tomato that cause softening so that farmers can allow the tomato to stay on the vine for a few days longer than regular supermarket tomatoes which are picked when they are green and later exposed to the ethylene gas in order to induce redness. The few extra days thatt he Flavr Savr stays on the vine allows sugars to be transported to the fruit which makes the tomato taste better. Regular tomato varieties can ripen on the vine too, but they cannot be transported without being damaged. The Flavr Savr, however, remains firm after being picked and also has a longer shelf life than regular supermarket tomatoes.
6. http://biotechknowledge.com/showlib_fr.cgi?644
Le débat sur les bénéfices et les risques éventuels de l'utilisation des organismes génétiquement modifiés (OGM) divise experts et acteurs de la filière alimentaire, avec d'autant plus d'acuité que les effets à long terme de cette révolution agronomique ne sont pas encore connus.
La transgénèse permet d'introduire un gène étranger sur une plante (maïs, soja, colza, betterave, coton etc.) pour la rendre résistante aux maladies, aux insectes ou aux herbicides. Cette technique peut également servir à augmenter la durée de vie des fruits et légumes ou à modifier la qualité nutritionnelle d'un aliment. Les promoteurs de l'utilisation du génie génétique en agriculture, au premier rang desquels les firmes agrochimiques qui ont mis au point ces plantes transgéniques, ne tarissent pas d'éloges sur les OGM. Le développement de plantes résistantes aux herbicides, aux insectes et aux virus permettra de reduire les traitements chimiques, ce qui constituera un plus pour l'environnement, déclarent les partisans des biotechnologies. Les pertes de production subies par les agriculteurs pourront être nettement diminuées, ajoutent-t-ils. Les partisans du génie génétique affirment que les pays en développement bénéficieront également de ces nouvelles technologies. Les chercheurs travaillent actuellement à la mise au point de plantes résistantes à la secheresse ou au sel. Certains industriels de l'agroalimentaire mettent en avant la possibilité d'"améliorer" par génie génétique la saveur des aliments. Des chercheurs japonais cherchent à neutraliser le caractère allergène du riz grâce au génie génétique. Mais cette nouvelle technologie présente des risques potentiels, que les pouvoirs publics et les experts s'efforcent d'évaluer. Ainsi, les adversaires des plantes transgéniques -écologistes mais aussi certaines associations de consommateurs et une partie des agriculteurs- soulignent que les mauvaises herbes risquent de devenir elles aussi résistantes aux herbicides, ce qui rendra leur élimination très difficile. De même, des inconnues démeurent sur la façon dont la faune microbienne du sol réagira dans ce nouvel environnement de plantes transgéniques.
Les opposants aux OGM craignent également l'apparition éventuelle d'allergies liées à la consommation de ces aliments. Ils s'inquietent également de l'utilisation de gènes de résistance aux antibiotiques à des fins de marquage dans certaines plantes génétiquement modifiées. Ils redoutent que cela n'entraine des phenomènes de résistance à ces antibiotiques chez l'homme.
Les dangers des OGM
1 / Dangers liés à la rupture de la barrière d'espèces
1.1 / Qu'est-ce que la barrière d'espèces
La fabrication de plantes transgéniques n'est pas, contrairement à ce qu'affirment ses défenseurs, la simple poursuite des procédés d'amélioration des plantes cultivées, utilisés et perfectionnés par les paysans depuis que l'agriculture existe. Jusqu'à l'avènement du génie génétique, l'amélioration des plantes, qui est en soit quelque chose de tout à fait légitime, respectait ce que nous appelons "l'ordre de la nature", puisqu'elle était contrainte par la reproduction sexuée des plantes et par la notion d'espèce. La manipulation génétique n'a en ce sens rien à voir avec un simple croisement, elle représente un saut qualitatif radical puisqu'elle permet de s'affranchir de la "barrière d'espèces", laquelle empêche par exemple un cheval de se croiser avec un chat. Les OGM sont des produits vivants manufacturés par l'homme. Grâce au génie génétique, nous avons construits des organismes qui n'auraient jamais existé dans la nature et dont le comportement est imprévisible.
1.2 / Risque de disparition de la notion d'espèce
Les manipulations génétiques permettent de prendre un ou plusieurs gènes d'une espèce quelconque et de les introduire dans une autre espèce. On peut ainsi, comme dans un Lego, prendre des pièces dansdifférentes espèces, et les assembler pour créer de nouvelles espèces. A la vitesse à laquelle évoluent ces sciences, qui jouent avec les mécanismes fondamentaux de la vie, il est à craindre que l'on obtienne dans un avenir proche des Frankenstein mi-animaux mi-végétaux. Le risque est donc de voir disparaître la notion même d'espèce. On ne
parlera plus de colza ou de maïs, mais d'organisme producteur de telle ou telle molécule.
1.3 / Perte de spécificité du monde agricole
L'agriculture intensive produit déjà des légumes ayant de moins en moins de goût, car les critères de sélection des espèces sont dictés par des impératifs industriels : arrivée prévisible à maturité, aspect, durée de conservation, résistance aux chocs pour les transports,... Il y a fort à craindre que les manipulations génétiques ne donnent un formidable coup d'accélérateur à ce processus. Dans un avenir proche, les légumes seront peut-être produits (et non plus cultivés) dans des usines, en l'absence de toute terre, ce qui commence déjà à se faire. La
différence entre paysan et ouvrier va s'estomper, l'agriculteur devenant un "moléculteur", un ouvrier spécialisé dans la production de substances nutritives ou pharmaceutiques. Outre le fait que les aliments produits auront moins de qualités gustatives, c'est tout le savoir-faire des paysans que l'on risque de perdre, basé sur des décennies d'observations et transmis au fil des générations.
1.4 / Les problèmes d'éthique
La conception des OGM pose de plus un grave problème d'éthique. Que, selon ses propres convictions ou sa culture, l'on se réfère à la volonté divine, à l'intangibilité des lois naturelles, au sens moral ou au simple bon
sens, avons-nous le droit d'interférer avec les mécanismes de la vie ? Consentirions-nous à manger une salade contenant des gènes humains ? Ce problème est quelque part similaire à celui du clonage. Certains chercheurs, lorsqu'ils ont commencé à entrevoir les mécanismes qui leurs permettraient de cloner les êtres humains, ont préféré pour des problèmes d'éthique stopper leurs recherches et ont demandé un débat public sur la bioéthique. D'autres chercheurs semblaient beaucoup plus préoccupés par les profits qu'ils pouvaient retirer de leurs travaux que par ces considérations philosophiques.
2 / Les risques écologiques
2.1 / Une pollution accrue de l'environnement
Dans le soja transgénique de la société américaine Monsanto, un gène introduit rend la plante tolérante à un herbicide dit total (car il tue toutes les plantes, bonnes ou mauvaises), le Roundup, commercialisé par la même société. Dans une culture naturelle, l'utilisation d'herbicides totaux est limitée car la plante cultivée en souffre également. Le soja étant rendu tolérant à l'herbicide Roundup, il est possible d'augmenter considérablement les doses, entraînant alors une pollution accrue des sols et des nappes phréatiques. Il faut signaler que les agriculteurs utilisant le soja de Monsanto ont l'obligation de n'utiliser que son désherbant, le Roundup. Ainsi, Monsanto vend ses semences transgéniques et augmente fortement ses ventes d'herbicide, ceci traduisant le souci de rentabilité des firmes agrochimiques au détriment de l'environnement et de la santé humaine.
2.2 / Implantation d'une plante en dehors de son écosystème naturel
Les mécanismes naturels de l'évolution ont amené chaque espèce a évoluer dans un écosystème particulier, c'est-à-dire en interaction avec une flore et une faune déterminées, dans des contextes géologiques et climatiques donnés. Implanter une espèce en dehors de son contexte originel conduit très souvent à des catastrophes écologiques. Ainsi, la Caulerpa taxifolia, dont quelques plants se sont retrouvés par erreur en Méditerranée, est en train de coloniser celle-ci. Elle supplante toutes les autres algues, provoquant la disparition de nombreuses espèces animales et végétales. Les risques sont similaires avec les OGM et spécialement les plantes transgéniques, car elles n'ont pas de passé évolutif, c'est-à-dire qu'elles n'ont pas évolué dans un écosystème donné, au milieu de leurs prédateurs naturels. Les plantes transgéniques ont pour but de mieux résister aux prédateurs ou aux parasites naturels, ce qui leur confère un avantage comparatif par rapport aux variétés naturelles locales et risque de conduire à la disparition de ces dernières et donc à un appauvrissement de la biodiversité. Cela est particulièrement grave, car ce sont ces variétés locales qui fournissent les ressources génétiques nécessaires pour améliorer les plantes cultivées, qui deviendraient par exemple victimes de nouvelles maladies. Signalons enfin le danger économique que représenterait la dépendance du monde agricole vis-à-vis d'une multinationale unique pour son approvisionnement en semences de maïs ou de colza.
2.3 / Extensions aux espèces voisines
On sait aujourd'hui que les plantes cultivées échangent, par croisements spontanés, leurs gènes avec les espèces sauvages apparentées, qui sont souvent de mauvaises herbes. On appelle cela le flux de gènes. En France, des études récentes menées à l'INRA (Institut National de Recherche Agronomique) ont montré que le gène de résistance à un herbicide implanté dans le colza pouvait se retrouver dans une mauvaise herbe apparentée, la ravenelle. Celle-ci devient alors fertile et insensible aux herbicides, une super mauvaise herbe. Ce flux de gène génère une "pollution génétique" qui, à l'inverse de la pollution chimique ou radioactive, est totalement irréversible. On ne pourra jamaisrapporter au laboratoire un gène qui se serait échappé de la plante génétiquement modifiée.
2.4 / Acquisition d'une résistance par les insectes
Les maïs transgéniques dont la culture est aujourd'hui autorisée en France contiennent un gène de la bactérie du sol Bacillus thuringiensis qui synthétise dans la plante une toxine, dite Bt, qui lui permet de se défendre contre un insecte : la pyrale du maïs. Contrairement à un insecticide classique, que l'on utilise à des moments précis, la plante transgénique produit la toxine en continu. L'insecte, étant au contact de cet insecticide d'une façon quasi permanente, va très vraisemblablement y devenir progressivement résistant. La toxine Bt sera alors inefficace à moyen terme et l'on devra de nouveau recourir aux insecticides toxiques que ces maïs devaient nous permettre d'éviter, augmentant ainsi la pollution des sols et des eaux, ou à de nouveaux maïs transgéniques. A moyen terme, ce processus recommencera et cette escalade aura pour seul résultat une pollution accrue de 'environnement. Parallèlement, le maïs transgénique conduira à la perte de l'agriculture biologique car la toxine Bt d'origine bactérienne est un des seuls insecticides autorisés dans les cahiers des charges de l'agriculture biologique.
2.5 / Les OGM en tant que vaccins
On parle actuellement beaucoup de manipuler génétiquement des plantes pour y introduire des vaccins. Le principe est assez simple : on introduit dans une plante un gène qui va produire une substance permettant de
vacciner contre une maladie spécifique celui qui mange la plante. Ce principe est séduisant, mais si des plantes contenant ces vaccins sontdisséminées dans la nature et transmettent leurs gènes à d'autres plantes ou animaux, des quantités très importantes de ces vaccins peuvent se retrouver dans la nature. On ne sait pas comment y réagiront certains organismes, et il est à craindre que ces vaccins, présents en trop grandes quantités dans la nature, deviennent inopérants (ce qui se passe actuellement avec les antibiotiques).
3 / Les risques alimentaires
Les risques alimentaires sont peu connus car ils n'ont été que très peu
étudiés. C'est donc le principe de précaution qui doit s'imposer.
3.1 / De nouvelles allergies
Les allergies alimentaires sont provoquées par les protéines, qui sont le produit d'expression des gènes. Introduire de nouveaux gènes dans un organisme, donc de nouvelles protéines, va accroître les risques d'allergies. Les risques sont aggravés du fait de l'adjonction de gènes en provenance d'organismes n'entrant pas ans la consommation alimentaire usuelle. Si l'exemple de l'introduction d'un gène de banane dans une tomate, pris souvent en exemple par les défenseurs des OGM, semble présenter des risques limités, il n'en est pas de même si le gène provient d'un scorpion ou d'un pétunia. Les scientifiques nous ont assuré que les risques étaient infimes, du fait des gènes utilisés. Cela a malheureusement déjà été contredit, malgré le caractère récent des manipulations génétiques. La société Pioneer, première compagnie semencière mondiale, a produit un soja plus riche en méthionine, acide aminé essentiel qui n'est pas produit naturellement par l'homme. Pour ce faire, elle a rajouté à ce soja un gène en provenance de la noix du Brésil. Des tests en laboratoire ont été faits pour vérifier que ce nouveau soja ne présentait pas de caractère allergène particulier, ils ont tous été négatifs. La noix du Brésil étant connue pour son puissant caractère allergène, des tests plus poussés ont été effectués, à partir du sérum sanguin de personnes présentant cette allergie. On s'est alorsrendu compte que les personnes allergiques à la noix du Brésil étaient également allergiques à ce soja manipulé. Il n'a donc jamais été commercialisé. Cela démontre cependant le peu de fiabilité des tests faits en laboratoire. Or, pour la majorité des manipulations génétiques, ces tests en laboratoire sont les seuls faisables, simplement parce qu'on ne connaît pas de consommateurs allergiques au scorpion ou au pétunia. Le public servira donc de cobaye malgré les risques encourus. Chaque jour, on découvre de nouvelles allergies à de nouveaux produits. On sait relativement peu de choses sur ces allergies, les causes et les circonstances de leur apparition. Il serait dans cette optique prudent de ne pas en augmenter inutilement les risques.
3.2 / Présence d'antibiotiques dans les OGM
Parmi les gènes introduits dans le maïs transgénique de Novartis, autorisé à la culture en France, se trouve un gène de résistance à un antibiotique commun, l'ampicilline. Ce gène est un marqueur, c'est-à-dire qu'il permet d'identifier les plantes ayant intégré les gènes d'intérêt (de synthèse de la toxine Bt dans le cas du maïs). Ce gène n'a ensuite plus aucune fonction, mais Novartis n'a pas jugé utile de l'extraire des plantes transgéniques. Les études menées par l'OMS (Organisation Mondiale de la Santé) sur les antibiotiques montrent que ceux-ci deviennent de moins en moins efficaces, les bactéries qui y sont soumises devenant insensibles au bout d'un certain temps. De nombreux scientifiques craignent que ladissémination de gènes de résistance aux antibiotiques à partir des plantes génétiquement manipulées n'accélère ce processus entraînant l'apparition de bactéries pathogènes contre lesquels les antibiotiques seraient impuissants. Il faut souligner que les antibiotiques sont les seules armes efficaces que nous possédons contre elles, que la recherche peine à trouver de nouvelles molécules efficaces et que les maladies hospitalières liées aux résistances aux antibiotiques tuent 10 000 personnes par an.
4 / Le manque de recul
Les dangers représentés par les OGM doivent s'apprécier en tenant compte du caractère très récent des développements de la transgénèse. Ce que la nature a mis plusieurs milliards d'années à construire, des hommes sont prêts à le contrarier en quelques années. La structure de l'ADN, support moléculaire de l'hérédité, n'est connue que depuis 1953. Les enzymes de restriction, ces sortes de ciseaux chimiques permettant de couper des portions d'ADN et de les insérer dans l'ADN d'un autre organisme, n'ont été découvertes que dans les années 70. La première plante transgénique, un tabac résistant à un antibiotique, a été créée il y a quinze ans seulement, et la première commercialisation d'une plante transgénique date de 1994, sans qu'il y ait eu de recul par rapport à des phénomènes qui peuvent avoir des conséquences écologiques, économiques, sociales et éthiques considérables. La transgénèse s'apparente aujourd'hui à une espèce de bricolage, où l'on "essaie et on voit ensuite" . On connaît encore relativement peu de choses sur l'ADN, sur le rôle et le fonctionnement des gènes, leurs interactions, et surtout sur les introns, des gènes aux fonctions inconnues et qui représentent environ 80% de l'ADN. Malgré l'imperfection des connaissances en génie moléculaire, malgré l'impact potentiel des disséminations de ces plantes manipulées, dans aucune autre discipline les applications commerciales ne suivent d'aussi près les découvertes scientifiques, qui deviennent le baromètre de la santé des multinationales à la bourse.
8. http://biotechknowledge.com/
A côté des avantages indéniables des aliments transgéniques, il y a le revers possible de la médaille. Une face oú certains craignent de voir se profiler quelques problèmes de santé et d'environnement.
"Avec le transgénique, on donne en quelque sorte naissance à ce que la nature ne peut pas créer", résume Willy Moens, chercheur au service de biosécurité de l'Institut Scientifique de la Santé Publique Louis Pasteur. "Les champs d'application ouverts sont donc énormes et... ont été très peu explorés jusqu'ici. Bref, rien ne permet au scientifique que je suis de dire avec certitude si tel ou tel aliment composé de susbtances végétales génétiquement modifiées posera ou non un problème au consommateur ou à l'environnement dans un avenir plus ou moins éloigné. Il faut prendre du recul. Et observer l'évolution de la situation sur le terrain". Explosion en 2000. Une mission d'observation que l'Institut scientifique de la santé publique Louis Pasteur (anciennement baptisé Institut d'Hygiène et d'épidémiologie) remplit déjà depuis près de dix ans dans de nombreux domaines, dont celui des... transgéniques. En matière de manipulations génétiques, les plus gros progrès sont toutefois très récents. Une difficulté rendue encore plus aiguë avec le déferlement de produits en provenance des Etats-Unis. Les problèmes posés en terme de contrôle seront alors énormes. "Les autorités sont déjà débordées avec le soja et le maïs transgéniques. Pensez à la situation que va engendrer la centaine de plantes génétiquement modifiées qu'on devrait voir déferler des Etats-Unis d'ici un ou deux ans", note Willy Moens. Faute de recul, on est dès lors contraint à se reporter sur des anticipations. Celles de Ciba-Geigy, de Monsanto et de Dupont de Nemours qui annoncent des lendemains qui chantent. Celles aussi des opposants farouches des OGM qui augurent, au contraire, des lendemains qui déchantent. Chez Greenpeace par exemple, on envisage au moins trois grands cas de figure. "Admettons qu'un consommateur soit allergique au tournesol. Dès qu'il consommera de la margarine au germe de soja génétiquement croisé avec un gène du tournesol, il tombera assurément malade. Sauf s'il est mis clairement au courant de la composition exacte du produit par le producteur. Ce qui n'est pas toujours évident", indique Pierre Coulon, permanent chez Greenpeace.
Deuxième risque: celui de la surenchère. "Ciba-Geigy vient de commercialiser une variété de maïs résistant au pyrale grâce à l'introduction d'un gène de Bacillus thurigensis dans sa structure macromoléculaire. Imaginons un instant que les insectes s'accommodent progressivement à la toxine bactérienne (ndlr: cela a été le cas des moustiques avec le DDT). Il faudra ensuite recourir à une bactérie plus agressive ou à un nouvel insecticide artificiel".
Bref, le risque est grand d'assister à une sorte d'escalade. Et de voir les insectes s'habituer à nouveau à la nouvelle toxine... Imaginons au contraire que la culture de ce même maïs se généralise au niveau de toute une région, d'un pays, d'un continent voire du monde entier et que les insectes ne s'accoutument pas à la toxine intégrée par manipulation génétique. La situation n'est guère plus enviable: on assisterait à la disparition de ces insectes, faute de nourriture. Avec le risque de voir les prédateurs de ces mêmes insectes disparaître à leur tour...
Les OGM font-ils peur ?
Pour rappel, est transgénique tout organisme - bactéries, plantes, etc... auquel on a greffé un ou plusieurs gènes. Par cette manipulation, il acquiert des nouveaux caractères héréditaires. L'adjectif est devenu célèbre, d'abord en France, en raison des tribulations du maïs produit par la firme Novartis. Si on en croit un sondage récent réalisé par Eurobaromètre dans 18 pays européens, une personne sur deux affirme appréhender les risques associés aux recherches en biotechnologies. Mais ils sont 15% à s'avouer ignorants sur le sujet.
()
Selon le Pr Guy-Grand, le développement des biotechologies est une évolution sans doute inévitable. Elles sont susceptibles d'améliorer non seulement les rendements agricoles mais aussi la qualité nutritionnelle, la sécurité alimentaire, voire les caractéristiques organoleptigues des aliments. Encore faut-il que ces progrès soient mieux expliquè au public et que ce dernier se sente protégé par une réglementation exigeante.
LE QUOTIDIEN - Les organismes génétiquement modifiés issus des biotechnologies sucitent toujours beaucoup de débate dans l'opinion publique.
Qu'en pensez-vous?
Pr Bernard GUY-GRAND : Ce débat est sain : il devrait permettre de diffuser sereinement une information objective auprès des faiseurs d'opinion (en l'occurrence les médecins) et du public. Les possibilités offertes par les biotechnologies sont immenses. Elles ne sont limitées que par l'acceptablilité des consommateurs, l'ethique professionnelle des industriels et la responsabilté des pouvoirs publics en matière de sécurité alimentaire.
On a toujours admis les "manipulations" génétiques des plantes : personne ne s'est jamais offusqué de voir créer de nouvelles variétés par hybridation, permettant d'obtenir de meilleurs rendements agricoles (indispensables compte tenu de la croisance des populations à nourrir), un colza dépourvu d'acide érucique (toxicité cariaque), des tomates d'apparence superbe (mais au goût fade), etc.
Le transfert de gène permet de faire la même chose et même beaucoup plus, avec un niveau de précision pratiquement jamais atteint : gain de temps, d'efficacité et de sécurité. Aujourd'hui, certains consommateurs semblent toutefois ne pas percevoir ces bénéfices qui sont pourtant impressionnantsÏ comme si leur allure "prométhéene" les inquiétait. Dans le domaine pharmaceutique, les biotechnologies ne sont pas contestées tant leurs avantages sont percus : si l'on avait eu plus tôt l'hormone de croissance recombinante, on aurait évité de transmettre la maladie de Creutzfeldt-Jakob aux déficits hypophysaires, etc. Dans le domaine agroalimentaire, une peur irraisonnée se fait jour. Pourtant, les bénéfices des biotechnologies pour le citoyen consommateur se situent au moins à deux niveaux: colectif, car les plantes transgéniques peuvent assurer une meilleure protection de l'environnement (moindre utilisation des phytosanitaires et/ou d'herbicides non rémanents avec la culture de plantes devenues "spontanément" résistantes ou tolérantes) et individuel, avec une amélioration des aliments, une sécurité alimentaire accrue, voire de meilleures caractéristiques organoleptiques.
Quels sont les bénéfices que l'on peut attendre dans le domaine de la nutrition?
Valeur nutritionnelle d'abord: on peut envisager - et c'est en cours - d'augmenter la teneur en acides gras polyinsaturés des oléagineux, de rendre les huiles végétales plus stables à l'oxydation, de modifier l'amidon des pommes de terre pour que les frites soient moins grasses, d'augmenter la teneur en acides aminés essentiels des végétaux qui en contiennent trop peu (lysine des céréales), etc. J'ai toujours pensé que c'est plus en modifiant les aliments qu'en tentant d'agir sur les comportements alimentaires que l'on assurerait les évolutions nutritionnelles nécessaires.
Sécurité alimentaire ensuite : les produits alimentaires issus des biotechnologies sont soumis à un ensemble de procédures de contrôle d'une sévérité que n'ont jamais connue les aliments traditionnels et qui se rapprochent de celles précédant les AMM médicamenteuses. Certes, elles ne peuvent prétendre être sans faille: qui se targuerait d'assurer le risque zéro pour quoi que ce soit! Du moins le risque est-il réduit au minimun, et aprés l'afaire du sang contaminé et de la vache folle, il serait étonnant qu'une vigilance accrue de la part de autorités ne soit pas de mise! De plus, ne perdons pas de vue que les biotechnologies peuvant améliorer la tolérance des aliments, en supprimant par exemple les allergenèes responsables d'allergies alimentaries (le riz au Japon en est un exemple).
Caractéristiques organoleptiques enfin. Si les plantes transgéniques, fruits ou légumes principalement, perdaient leurs qualités gustatives...quel échec pour le marché! Les tomates dont la maturité est retardée par transgenèse (avantage pour le transport et la réduction des pertes) ne valent peut-être pas nos bonnes marmandes. Mais l'histoire des pommes golden ausi belles de forme que médiocres de goût montre que la sélection génétique n'a pas attendu la transgenése pour se fourvoyer. Aux consommateurs d'être vigilants et aux producteurs...de modifier les golden pour qu'elles soient belles et bonnes.
Quoi qu'il en soit, l'acheteur a le désir légitime de savoir; s'il n'a pas l'impression - fausse le plus souvent - qu'on lui cache quelque chose, il n'aura guére de raison de refuser. Peut-on imaginer que les pays défavorisés puissent un jour profiter de ces techniques?
Oui sans doute, car l'amélioration de certaines qualités permettra de reprendre des cultures locales dans des sols peu favorables. Il serait dés lors possible de pallier les carences nutritionnelles de ces populations, de respecter les traditions alimentaires et de permettre une certaine indépendance vis-a-vis des pays industrialisés.
Les biotechnologies modernes constituent un progrés indéniable pour tous les acteurs de la chaine alimentaire, des semenciers aux consommateurs qui devraient pouvoir en partager les fruits. Il faut bien sûr disposer d'une réglementation précise, ce qui est maintenant le cas, et en contrôler l'application et le respect. Il semble que les Suisses, en repoussant par référendum un projet d'interdiction des biotechnologies, aient montré la voie de la sagesse.
B. Livres
9. Campbell
/ pp. 410-413 et 764-765
à voir annexe I
10. Biologie évolution, diversité et environnement
S. Mader / pp. 190-203 et pp.206-207
Etant donné que les informations que ce livre nous a apportés représentaient le cours, il ne nous a pas paru utile de copier les extraits utilisés.
C. Brochures, journaux, etc.
11. Le génie génétique, c'est quoi ?
L'Hebdo
à voir annexe II
12. Génie génétique Chance et défi pour la médecine
Académie suisse des sciences médicales / pp. 1-9
à voir annexe III
13. Nutritio
Nestlé / p.6
()
La tomate Flavr Savr
La tomate vient en tête dans la production mondiale de légumes. Le fruit mûr, pleinde saveur, est trop délicat pour supporter de longs transports. Par conséquent, on cueille des tomates vertes que l'on fera mûrir à leur lieu de destination. Pour créer la tomate Flavr Savr, on a commencé par identifier le gène responsable de la dégradation des parois cellulaires, puis on a construit un gène antagoniste que l'on a introduit dans la cellule. Ce gène existe donc en deux versions dans le patrimoine génétique de la tomate, l'une positive, l'autre négative. Lorsqu'on les active, ces deux copies s'annulent réciproquement. Le processus qui conduit au ramollissement du fruit est ralenti par rapport au processus de maturation. La tomate peut donc être cueillie une semaine plus tard et développer ainsi toutes ses qualités. ()
D. Film
14. USA Autour de l'agriculture
ARTE
IV. Analyses et conclusions
vant de se lancer dans les explications des techniques du génie génétique, il faut connaître les " ancêtres " des procédés actuels. Voici donc une brève rétrospective des techniques connues autrefois accompagnée de quelques définitions indispensables, puis des explications sur les méthodes actuelles du génie génétique, avec l'étude approfondie de la tomate transgénique.
Brève chronologie du génie génétique
Un gène détient toutes les informations nécessaires à créer une protéine (les protéines sont " la matière première " qui constituent les êtres vivants). Un gène est donc responsable d'un caractère particulier (forme du nez, couleur des yeux,) que nous tenons de nos parents, grand-parents, etc. C'est sur l'ADN (substance chimique qui forme les chromosomes) que reposent les gènes que possèdent n'importe quel organisme vivant. L'homme possède 46 chromosomes (ou 2 pairs de 23 provenant de nos deux parents), présents dans le noyau de chacune de nos cellules qui forment les tissus de notre corps. Lorsque l'on parle de l'ensemble de nos gènes (ou de tout organisme ), il s'agit du génome, c'est-à-dire l'ensemble de l'information génétique (héréditaire), le patrimoine génétique.
Le génie génétique proprement dit modifie le génome d'un organisme végétal, animal ou microscopique (bactéries, levures,). Si le génie génétique date de peu, c'est aussi un sous-domaine de ce qu'on appelle les biotechnologies. Cet ensemble de techniques permet de produire des substances utiles à l'homme ou de lui rendre des services, en se servant des cellules animales ou végétales ou des micro-organismes. Les biotechnologies commencent chez les peuples de Moyen-Orient au Ve millénaire avant J.-C., dans la fabrication de la bière. La fermentation relève en effet des biotechnologies, c'est ainsi que plus tard on produira du vin, du pain, du fromage, des yaourts, etc.
Mais ce n'est qu'en 1865 que l'on découvrira les lois de l'hérédité grâce aux travaux du moine Mendel. Puis l'on découvre les gènes (1915), la forme de l'ADN (1953), etc., pour en arriver finalement à la première expérience utilisant les techniques du génie génétique (1973). En 1982, on " crée " le premier animal transgénique, puis des aliments génétiquement modifiés (1983). Mais ce n'est qu'en 1994 qu'apparaît le premier aliment transgénique dans le commerce (américain) : la tomate Flavr-Savr, dont nous parlerons précisément plus loin (en même temps se développe la recherche pour de nouvelles thérapies et médicaments par le génie génétique). Des biotechnologies qualifiées de traditionnelles (fermentation, sélection de plantes,), on passe à une technologie plus poussée et plus précise qui fait appel au génie génétique. [cf. docs 10-11]
Application sur les organismes végétaux
Le secteur agroalimentaire connaît de nombreux facteurs qui peuvent abîmer ou détruire les récoltes de céréales, fruits et légumes. Il existe beaucoup de virus, de bactéries mais aussi d'insectes qui s'attaquent aux cultures. C'est pourquoi il faut utiliser des herbicides, pesticides et autres fongicides que les plantes ou le sol ne supportent pas toujours bien.
Cependant, on s'est rendu compte que certaines plantes résistaient à, par exemple, des insectes ou à des microorganismes pathogènes. Certains organismes produisent des toxines qui anéantissent des insectes, ou qui créent des anticorps contre un pesticide (ce sont des caractères d'un organisme). Ces substances sont en fait crées indirectement par les gènes ; ces derniers codent les protéines qui sont responsables de la synthèse des substances utiles.
C'est là qu'interviennent les techniques du génie génétique. Si l'on parvient à isoler un gène précis qui est la base de l'expression du caractère recherché (p.ex. résistance à un insecte, à un herbicide), on peut l'extraire de l'organisme et le transmettre dans un autre organisme.
Lorsque l'on établit la " carte génétique " d'un organisme végétal, on repère le gène responsable d'un caractère non désiré ou le gène responsable d'un caractère intéressant (p.ex. synthèse d'une toxine utile) ; il faut, bien sûr, déterminer au préalable la protéine codée par ce gène. Par la suite, on extrait ce gène d'intérêt (qui peut provenir d'une bactérie, d'un champignon, d'un autre organisme végétal ou d'une autre variété d'une même espèce) par des manipulations génétiques. Des enzymes appelés enzymes de restriction coupent l'ADN à un endroit précis (un enzyme est spécifique pour couper à tel endroit, lorsque il rencontre tels nucléotides formant les bases de l'ADN) et à présent, le gène et les séquences d'ADN nécessaires (promoteur et terminateur, autrement dit " bouts collants ") sont isolés (cf. fig. 1). Ce transgène va maintenant pouvoir être inséré dans la plante voulue, par le biais de la transgénèse.Il existe deux principales techniques de transgénèse : le transfert indirect et le transfert direct :
Il concerne les plantes dicotylédones (" végétaux qui possèdent deux feuilles embryonnaires "). Le gène d'intérêt isolé est inséré dans une bactérie particulière nommée Agrobacterium tumefaciens ; c'est une bactérie recombinante. Une bactérie contient un plasmide, filament d'ADN qui ne se situe pas dans le noyau de la cellule (contrairement aux cellules des organismes pluricellulaires). Ici de nouveau, un enzyme de restriction va couper le plasmide. On insère alors le transgène dans la bactérie susmentionnée : le fragment d'ADN portant le gène d'intérêt va se coller grâce au bouts collants au plasmide ouvert.
Le plasmide de l'Agrobacterium tumefaciens est appelé plasmide Ti ; lorsqu'il entre en contact avec une plante, il transmet à l'ADN du noyau d'une cellule de son hôte une partie de son plasmide : il transfert son matériel génétique. Ainsi, quand la bactérie contient dans son plasmide un gène intéressant, les cellules de la plante possèderont aussi le gène désiré (cf. fig. 2).
Le plasmide de l'Agrobacterium tumefaciens n'infecte pourtant pas les plantes monocotylédones (une seule feuille embryonnaire), telles que le blé, le maïs, le soja etc. Dans ce cas, on utilise la biolistique,c'est-à-dire le transfert direct de l'ADN. Le gène isolé est projeté dans le noyau de la cellule végétal par le biais d'un " pistolet " à gènes ; on tire des microbilles métalliques portant l'ADN qui traversent la membrane cellulaire, rendue perméable au préalable par éléctroporation ou par un traitement au polyéthylène glycol (agent chimique).
Une fois que le gène d'intérêt fait partie du génome de l'organisme, les variétés descendantes - selon les lois de l'hérédité - seront porteuses du gène qui leur confère un caractère dont elles étaient auparavant démunies. En effet les premières cellules modifiées se divisent et créent de nouvelles cellules avec le nouveau gène ; il s'agit des cellules somatiques (qui forment les tissus), mais aussi germinales, qui transmettront le nouveau gène aux plantes descendantes. On peut alors dire qu'il s'agit d'un organisme génétiquement modifié (O.G.M.), car le patrimoine de la variété de base a été transformé.
Après toutes ces manipulations délicates et compliquées à réaliser, on peut étudier précisément le rôle du transgène introduit, en observant les nouveaux caractères de la plante. [cf. docs 1-3-9-11]
3. Exemple d'organisme génétiquement modifié : la tomate Flavr Savr
Le premier aliment génétiquement modifié apparaissant dans le commerce a été la tomate Flavr Savr, mise en vente dès 1994 dans les supermarchés aux Etats-Unis puis en Grande-Bretagne. Cette tomate possède un caractère bien particulier : elle peut se conserver bien plus longtemps qu'une tomate ordinaire. Mais dans quel but a-t-on modifié ce légume ? Comment les techniciens ont-ils mis au point cette tomate ? Et finalement, à qui profite vraiment ce produit ?
Dans quel but ?
 Aux USA comme dans la plupart des pays, les tomates que l'on peut acheter dans les supermarchés sont cueillies encore vertes pour le transport. Si on les cueillait déjà mûres et rouges, le transport vers les magasins serait tout simplement impossible, les légumes auraient
Aux USA comme dans la plupart des pays, les tomates que l'on peut acheter dans les supermarchés sont cueillies encore vertes pour le transport. Si on les cueillait déjà mûres et rouges, le transport vers les magasins serait tout simplement impossible, les légumes auraient
été complètement détruits avant l'arrivée. Naturellement, la saveur de ces tomates (artificiellement) mûries après la cueillette n'est pas comparable à des tomates de jardin portées à maturation sur la plante. C'est pourquoi des chercheurs de la société agroalimentaire Calgene de Davis en Californie ont tenté de créer la tomate " parfaite " (cf. fig. 3) : une tomate qui puisse mûrir sur la plante sans pour autant devenir plus fragile.
La firme américaine a donc investi 25 millions de dollars pour mettre au point cette tomate réalisée après une dizaine d'années de travail. Contrairement à d'autres aliments transgéniques, la tomate a été modifiée par génie
génétique pour résister non pas à un insecte , à un pesticide, ou à un microorganisme pathogène, mais aux manipulations des humains. On a créé la Flavr Savr afin de ralentir le processus de maturation de la tomate et de pouvoir ainsi la laisser développer ses qualités dans les champs, sans pour autant qu'elle ne soit fragile et impossible à transporter. [cf. docs 2-13-14]
Par quels manipulations ?
Le chercheurs de cette société ont avant tout dû établir le génome de la tomate et ainsi ont pu déterminer quel gène était responsable de la production d'un enzyme (protéine) bien particulier : l'enzyme (du moins la plus importante de celles) qui dégrade les parois cellulaires de la tomate, ou autrement dit, qui la fait mûrir puis pourrir. Il s'agit de l'enzyme polygalacturonase.
En fait, l'ADN sur lequel repose le gène en question transcrit un ARN messager (ARNm) qui amène l'information que porte l'ADN dans le cytoplasme. L'ADN est une substance chimique d'une structure en " double hélice " qui est composée de deux brins (formés de désoxyrhybose et de phosphate) reliés par des bases (formées d'adémine, etc.) (l'ensemble d'une base, de désoxyrhybose et de phosphate et appelé nucléotide). Quant à l'ARN, il contient la même information génétique à la seule différence qu'il n'est composé que d'un seul brin (formé de nucléotides légèrement différents) appelé complémentaire, car il possède des nucléotides complémentaires à ceux de l'ADN. L'un des brins d'ADN s'apparie avec un brin d'ARN pour créer un ARNm : ce processus est appelé transcription. Cette ARNm quitte le noyau pour atteindre le cytoplasme, où les codes génétiques pourront être " lus " par un ribosome (traduction) ; finalement, on arrivera à la fin du processus de synthèse et une nouvelle protéine sera créée.
Les scientifiques ont donc cloné le gène de tomate codant pour la protéine responsable du ramollissement en extrayant l'ADN. Et c'est là qu'intervient toute la magie du génie génétique : ils ont " fabriqué " et cloné un gène qui possède les bases d'ADN complémentaires à celui des bases de l'ADN du gène responsable du ramollissement. Ce gène " antisens " ou gène antagoniste est introduit dans le génome de la tomate par vecteur biologique, par le biais de la transgénèse indirecte (cf. point IV.2 / p. 23).
Dès lors le mécanisme est logique : lorsque les deux gènes (celui du ramollissement et sa copie complémentaire) transcrivent un ARN messager, l'ARNm " normal " se lie à l' ARNm complémentaire et ce dernier bloque la traduction. L'enzyme qui mène au pourrissement n'est plus fabriquée (en quantité négligeable), et donc la tomate ne pourrit plus (en tout cas moins vite) (cf. fig. 4).
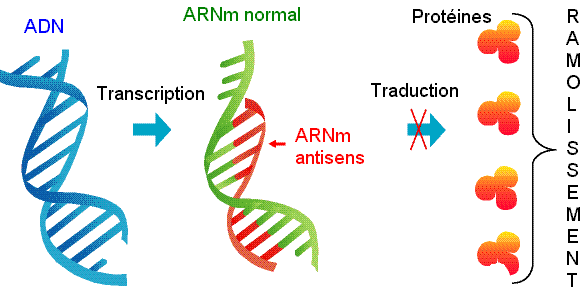 On peut à ce moment-là cultiver des tomates et les laisser mûrir et devenir rouge sur la plante, mais comme l'enzyme qui accélère le mûrissement de la tomate est inhibé, le fruit reste encore ferme et transportable jusqu'au supermarché. Le quelques jours supplémentaires de la tomate sur le plant permet aux fruits de développer toutes ses qualités et d'obtenir un goût meilleur à celles cueillies vertes.
On peut à ce moment-là cultiver des tomates et les laisser mûrir et devenir rouge sur la plante, mais comme l'enzyme qui accélère le mûrissement de la tomate est inhibé, le fruit reste encore ferme et transportable jusqu'au supermarché. Le quelques jours supplémentaires de la tomate sur le plant permet aux fruits de développer toutes ses qualités et d'obtenir un goût meilleur à celles cueillies vertes.
Normalement, on cueillait les tomates vertes et on les faisait mûrir à leur lieu de destination en leur injectant de l'éthylène, une hormone gazeuse produite par les végétaux qui porte le fruit à maturation. Maintenant les tomates sont cueillies rouges et l'éthylène peut faire mûrir la plante de manière naturelle. [cf. docs 4-5-9-10-14]
A qui profitent ces modifications ?
Si le but " technique " de la Flavr Savr (maturation retardée) est clair, on peut par contre se demander à qui revient le bénéfice de ces manipulations coûteuses. Car il est clair que ce n'est pas le consommateur qui a demandé cette nouvelle tomate.
Un des reproches majeurs faits à cette tomate était son goût de carton. Les généticiens ont alors identifié le composant chimique de la tomate et l'on renforcé pour que ce goûtlà soit prépondérant dans le palais du consommateur.
A la base, les chercheurs ont créé la Flavr Savr pour que le transport soit facilité. Or le transport était déjà facile, puisque les tomates vertes sont aisément manipulées. Donc on aurait créé cette tomate pour le consommateur, pour qu'il puisse manger une tomate mûrie non-artificiellement. Mais dans une autre vision, peut-être cette tomate a été créée pour que l'on ait pas à la traiter à l'éthylène après la cueillette, opération sans doute coûteuse.
En définitive, cette tomate ne profite en rien à l'agriculteur qui la cultive et l'amène au supermarché. Cependant, le supermarché, lui, limite ses pertes, car la tomate peut rester plus longtemps dans le magasin, étant donné le pourrissement retardé. Si l'on admet cela, l'argument " tomate meilleure " en faveur du consommateur est un argument illusoire pour appâter le client La Flavr Savr a donc été mise au point plutôt pour les gérants des supermarchés. [cf. docs 13-14]
4. Risques et avantages des plantes génétiquement modifiées
 Des plantes dotées d'un gène qui résiste aux ravages des insectes, des anomaux qui produisent des médicaments, des brebis reproduites par clonageLe génie génétique progresse à pas de géant, passant par le stade du laboratoire aux applications économiques. Mais la polémique scientifique et médiatique fait rage. Les uns nous vantent une société d'abondance où les récoltes seront multipliées, où le bétail produira plus de lait, plus de viande. Les autres prédisent un univers complètement différent où les manipulations génétiques menaceront santé et environnement. Le débat freinera-t-il l'essor de ces technologies, sur lesquelles certains groupes comme Monsanto ou encore Novartis ont misé gros ? (cf. fig. 5) En effet comme tout le monde l'aura compris les enjeux industrielles et agricoles sont énormes.
Des plantes dotées d'un gène qui résiste aux ravages des insectes, des anomaux qui produisent des médicaments, des brebis reproduites par clonageLe génie génétique progresse à pas de géant, passant par le stade du laboratoire aux applications économiques. Mais la polémique scientifique et médiatique fait rage. Les uns nous vantent une société d'abondance où les récoltes seront multipliées, où le bétail produira plus de lait, plus de viande. Les autres prédisent un univers complètement différent où les manipulations génétiques menaceront santé et environnement. Le débat freinera-t-il l'essor de ces technologies, sur lesquelles certains groupes comme Monsanto ou encore Novartis ont misé gros ? (cf. fig. 5) En effet comme tout le monde l'aura compris les enjeux industrielles et agricoles sont énormes.
Les plantes transgéniques cherchent toutefois plus à faire leurs preuves dans les champs que dans l'assiette du consommateur. Car le débouché le plus immédiat est agricole. Le débat sur les bénéfices et les risques éventuels de l'utilisation des organismes génétiquement modifiés (OGM) divise experts et acteurs de la filière alimentaire, avec plus d'intensité que les effets à long terme de cette révolution agronomique ne sont pas encore connus. Tout organisme est sujet à des modifications de son patrimoine génétique, qui sont à la base de la théorie de l'évolution. Toutefois les techniques modernes permettent d'accélérer ce processus naturel et soulèvent de nouveaux problèmes. Ces nouvelles technologies posent des questions de sécurité , de qualité et d'éthique. Elles ont leurs vices, elles ont leurs avantages : une grande quantité de questions se posent lorsqu'on évoque le génie génétiques. Les sondages sont révélateurs : Les gens ont des craintes ; Les aliments nouveaux seront-ils toxiques ? les transgènes vont-ils modifier toute la plante ? Est-ce qu'il y aura une nouvelle source d'allergies ? etc. [cf. docs 8-11]
Les modifications apportées, en permettant de franchir la barrière d'espèces, soulèvent de nombreuses questions sur les risques potentiels susceptibles d'apparaître :
 Bref les risques existent mais le développement des biotechnologies est une évolution sans doute inévitable et les apports du génie génétique, même s'ils sont actuellement diversement analysés , critiqués (cf. fig. 7) et utilisés suscitent beaucoup d'espoirs dans divers domaines. Voyons maintenant quels sont les avantages de ces manipulations dans le dans l'agriculture :
Bref les risques existent mais le développement des biotechnologies est une évolution sans doute inévitable et les apports du génie génétique, même s'ils sont actuellement diversement analysés , critiqués (cf. fig. 7) et utilisés suscitent beaucoup d'espoirs dans divers domaines. Voyons maintenant quels sont les avantages de ces manipulations dans le dans l'agriculture :
c) Des vaccins ! On parle actuellement beaucoup de manipuler génétiquement des plantes pour y introduire des vaccins. Le principe est assez simple : on introduit dans une plante un gène qui va produire une substance permettant de vacciner contre une maladie spécifique celui qui mange la plante. [cf. docs 8-11]
5. Opinions diverses sur le phénomène
Il n'est pas facile de prendre parti, de donner son avis sur un tel sujet, parce que personne ne peut prédire ce que vont devenir les plantes du futur. On ne peut que supposer des éventuels bénéfices, supposer toutes sortes de risques, supposer des catastrophes Chacun avance des arguments mais aucun est véritablement prouvé ; donc notre opinion se forge sur des idées qui nous accommodent. Le génie génétique fait énormément parler de lui car il est complexe, il concerne le futur et il demande de la mesure. Cette mesure se montre par les précautions que l'on prend : non seulement par le vote mais surtout par les nombreux débats (notamment sur Internet).
A ce stade du débat, on retouve de vieux opposants ; les groupes écologistes alternatifs (Greenpeace {cf. fig. 6}, WWF, les partis écologistes, ) face aux grandes entreprises (Novartis, Monsanto, Cibaz, Calgene, ) au seul but lucratif qui, malgré une certaine propagande en faveur de l'environnement, ne se soucie au fond d'elles-mêmes que peu du sort à long terme de la nature, et plus précisément, du sort de la biodiversité, de l'écosystème et des pions de la nature : nous, entre autre.
Par contre, le problème d'éthique lui n'a pas besoin du futur pour s'ouvrir à nous ! En effet, que l'on se réfère, selon ses propres convictions ou sa culture, à la volonté divine, à l'intangibilité des lois naturelles, au sens moral ou simple bon sens, avons-nous le droit d'interférer avec les mécanismes de la nature ? Certains chercheurs, lorsqu'ils ont commencé à entrevoir les manipulations qui leurs permettraient de cloner des êtres humains, ont préféré pour des problème d'éthique stopper leurs recherches et ont demandé un débat public sur la bioéthique. D'autres chercheurs semblaient beaucoup plus préoccupés par les profits qu'ils pouvaient retirer de leur travaux que par ces considérations philosophiques.
Plusieurs films comme Jurrasic Park parlent de ce sujet. Ce film libère un message : la vie prend son chemin avec ou sans les humains. Nous ne pouvons pas (encore) contrôler la nature tellement elle est complexe, ne jouons pas avec les gènes, la base même de la vie, sans prendre de précautions. Il faut en effet bien pesé le poids des bénéfices qui ne vont pas sans risques bien pesants eux aussi
Nous ne sommes pas contre le développement du génie génétique mais soutenons les renforcements de dispositifs de contrôle des plantes transgéniques et d'information des citoyens. A notre avis, le génie génétique ne doit pas favoriser les grandes sociétés agroalimentaires, mais plutôt l'amélioration de la nourriture en préservant l'écosystème. En définitive, cette science d'avenir doit favoriser l'agriculteur autant que le consommateur.
V. Bibliographie
A. URL (Internet)
3. http://www.jouy.inra.fr/actualites/dossiers/ogm.html
4. http://isip.com/antisens.htm
5. http://trc.ucdavis.edu/Coursepages /PLB105/students/Tomato/reproductive
/flavr.html
6. http://biotechknowledge.com/showlib_fr.cgi?644
8. http://www.biotechnowledge.com
B. Livres
9. Campbell,
10. S. Mader, " Biologie évolution diversité et environnement ", De Boeck, 1988,
pp. 190 à 203 et 206-207
C. Brochures, journaux, etc.
11. L'Hebdo, " Le génie génétique, c'est quoi ? ", éd. Ringiers Romandie, avril 1998, pp.2 /5 /10-12
12. Académie suisse des sciences médicales, " Génie génétique chance et défi pour la médecine ", 1998, pp. 1-7
13. Nestlé, " Nutritio ", 1.98, p. 6
D. Film
14. Arte, " USA Autour de l'agriculture ", Arte, 22.03.97 (disponible auprès des auteurs du rapport)